После эмболизации маточных артерий сколько на больничном листе
Опубликовано: 24.05.2026
Эмболизация маточных артерий редко приводит к осложнениям и доставляет не так много неудобств, которые к тому же со временем проходят. Но, конечно, пациенткам важно понимать, всё ли идёт по плану. Для этого мы выдаём памятки с основной информацией о том, что делать и не делать после ЭМА, а также чего ждать и когда позвонить своему врачу.
Здесь вы найдёте более полный вариант нашей памятки.
Повышенная температура после эмболизации
В первые сутки ЭМА температура, как правило, достигает 37,5-38 градусов. Нередко она может сохраняться до недели, но может также в редких случаях наблюдаться в вечернее время еще в течение 2-3 недель после вмешательства.
В отдельных случаях, когда узел имеет тенденцию к рождению (выходу из матки, это также называют «экспульсия», и о возможности этого результата вас обязательно еще до ЭМА предупредит наш гинеколог), температура может вновь повыситься, что укажет на начало экспульсии и будет сопровождать ее до полного выхода узла. Заметим, что экспульсия — это весьма благоприятный рузультат ЭМА, который возможен для узлов субмукозной локализации.
Боли после ЭМА
Сама процедура ЭМА совершенно безболезненна, однако после нее возникают боли, которые удается с успехом свести к тянущим ощущениям внизу живота, напоминающие боли при менструации. Конечно есть индивидуальные особенности, но большинство пациентов отмечают, что эти боли не приносят им выраженных страданий. Боли с меньшей интенсивность продолжаются и в последующие несколько дней и полностью стихают через 7–10 дней после ЭМА. С 3–4 дня после операции потребности в принятии обезболивающих препаратов практически не возникает.
Боли после ЭМА никак нельзя назвать «адскими» и вызывающими «болевой шок», как утверждают некоторые гинекологи, по непонятным причинам отговаривающие пациенток от ЭМА.
Что можно есть после эмболизации?
Лучше, чтобы первым приёмом пищи после ЭМА был ужин. Если поесть раньше, то может возникнуть тошнота. После возвращения домой можно есть, как обычно, много пить, есть больше клетчатки, так как обезболивающие могут стать причиной запора. Если вас тошнит или рвёт, это нормально, но доктору об этом нужно знать — он назначит подходящий препарат, чтобы убрать эти неприятные явления.
Когда можно принять душ?
В душ можно идти на следующий день после операции, однако в течение 5 дней стоит воздержаться от принятия ванны или плавания.
Сексуальная жизнь после лечения миомы методом ЭМА
Первый месяц после ЭМА лучше воздержаться от секса, однако это необязательная рекомендация. При нормальном самочувствии ею можно пренебречь.
Первые 1,5–2 месяца после ЭМА лучше использовать барьерную контрацепцию, то есть презерватив. После этого по назначению врача можно перейти на гормональные контрацептивы. Однако делать это стоит только после «рождения» узла.
Занятия фитнесом и физические нагрузки
Занятия спортом можно ограничить на месяц-полтора после ЭМА. Однако это не строгая рекомендация, так как научных оснований у неё нет — скорее, простая перестраховка и забота о самочувствии, но никак не об эффективности ЭМА: на результат эмболизации физические нагрузки не влияют.
Менструация
В большинстве случаев месячные после ЭМА приходят, когда и положено. Если эмболизация была выполнена незадолго до менструации, то кровотечение может быть достаточно скудным.
Раньше задержки в некоторых случаях составляли от месяца до полугода. Однако сейчас из-за применения эмболизационного препарата с более крупными частицами эта проблема практически исчезла.
В единичных случаях у женщин, находящихся на пороге менопаузы с характерными нарушениями менструального цикла, месячные могут не вернуться, то есть наступит климакс. Чаще такое бывает у женщин старше 45 лет. Однако в подавляющем большинстве случаев месячные постепенно становятся всё менее и менее обильными и к году превращаются в совершенно обычные. Если кровотечение усиливается после того, как нормализовалось, возможно, это связано с «рождением» узла. После экспульсии месячные должны стать умеренными. Между ними поначалу возможны более обильные прозрачные выделения, чем раньше. Со временем они уйдут.
«Рождение» (экспульсия) узла миомы
«Рождение» узла происходит обычно через 2–3 месяца после ЭМА, но это может случиться и через год и через несколько дней. О том, что в вашем случае предполагается такое развитие событий, вы узнаете ещё до эмболизации: это станет понятно при УЗИ. В большинстве случаев «рождаются» субмукозные узлы. Если миома небольшая (меньше 3–5 см), то обращаться к врачу за помощью нет необходимости. При больших узлах консультация гинеколога может понадобиться, но она проводится и удалённо. Обычно узел выходит сам, реже женщине необходима дополнительная медицинская помощь.
Рост миомы после ЭМА
После грамотно проведённой ЭМА кровоснабжение миом не может возобновиться, соответственно, расти они не могут. Другими словами узел погибает. Не чаще чем одном случае на 100 процедур возможно восстановление кровотока в узле с последующим его ростом, это связно с наличием дополнительных источников кровоснабжения узла, которые были не видны во время первого вмешательства. В таких случаях производится повторная ЭМА и этот сосуд подвергается эмболизации.
Возникновение новых узлов - рецидив миомы матки
Новые узлы после ЭМА возникают крайне редко — обычно если эмболизации была проведена не лучшим образом из-за сложной анатомии маточных артерий или недостаточной квалификации хирурга. Дело в том, что из-за особенностей сосудов, кровоснабжающих узлы, эмболизирующий материал доходит до всех, в том числе самых маленький миом.
Если тем не менее новые узлы выросли, то повторная эмболизация решает проблему. В нашем центре такие вмешательства проводятся бесплатно.
Беременность после эмболизации
По последним данным, эмболизация маточных артерий не противопоказана женщинам, которые впоследствии планируют забеременеть. Эндометрий (оболочка, выстилающая матку изнутри) может стать слишком тонким и препятствовать наступлению беременности лишь в том случае, если частицы эмболизационного препарата очень маленькие и закупорили мелкие ветки сосудистой сети матки. Но сейчас такие материалы практически не используются.
На вероятность наступления беременности при экстракорпоральном оплодотворении ЭМА не влияет.
Некроз матки
Некоторые гинекологи иногда пугают своих пациенток с миомами: «После ЭМА у тебя будет некроз матки, потом придётся удалять». Вероятно, эта идея связана с неверным представление о том, что происходит при эмболизации маточных артерий. Несмотря на то, что перекрывается кровоток в миомах, нарушения кровоснабжения самой матки не происходит: с ней связано достаточно других сосудов. Поэтому ни о каком некрозе, отмирании матки речи быть не может.
Изменения веса
Иногда на форумах можно встретить утверждения, что после ЭМА вы непременно поправитесь. Во-первых, что именно может привести к таким последствиям, неясно. Во-вторых, этот вопрос не изучался по той простой причине, что врачи не видят взаимосвязи между ЭМА и набором веса и с тем же успехом могли бы изучать ухудшение зрения после эмболизации маточных артерий. Если вы набрали вес после этого вмешательства, то лучше искать настоящие причины случившегося, иногда вместе с терапевтом или диетологом.
Варикозное расширение вен
Не существует никакой связи и никакого механизма, способного связать ЭМА и варикозную болезнь. К варикозному расширению вен нижних конечностей приводят разные причины. В частности наличие очень большой миомы матки, которая за счет компрессии может нарушать отток крови из нижних конечностей. В этом случае результат ЭМА — уменьшение размеров матки — может даже приводить к снижению выраженности хронической венозной недостаточности у пациентов с варикозной болезнью.
Работа
Уже на следующий день после операции подавляющее большинство пациенток отправляется домой. Обычно примерно через неделю-две все симптомы уходят и можно вернуться к привычным делам и выходить на работу.
Наблюдение
После ЭМА врач скажет, когда вам нужно будет снова ему показаться. В дальнейшем потребуется ещё несколько консультаций. Первое УЗИ обычно проводится через 3 месяца после ЭМА. Далее через 6 и 12 месяцев.
Позвоните своему доктору или запишитесь к нему на приём, если обезболивающие не помогают, температура выше 38,0 °C, появились необычные выделения из половых путей.
Спиридонова Н.В., Басина Е.И., Шатунова Е.П., Арутюнян К.Н.,Шахова И.В., Клыкова О.В.
Резюме
В настоящем исследовании произведен анализ течения раннего послеоперационного периода у пациенток с миомой матки, которым проводилась эмболизация маточных артерий. Оценивалась частота встречаемости постэмболизационного синдрома у данной группы пациенток и наиболее характерные его клинические черты.
Ключевые слова
Статья
Миома матки остается одной из самых распространенных патологий у женщин репродуктивного и климактерического возраста. Несмотря на незначительный риск малигнизации (менее 1%), основным методом лечения миомы матки остается хирургический (Кулаков В.И., Адамян Л.В., 2001; Савицкий Г.А., 2003). Одним из наиболее перспективных органосохраняющих направлений в лечении миомы матки является эмболизация маточных артерий (Адамян Л.В., 2002;Тихомиров А.Л. и др., 2004; Ravina J.H., 2004).
Целью настоящего исследования явилась оценка особенностей течения раннего послеоперационного периода (1-10 сутки) у пациенток с миомой матки, перенесших эмболизацию маточных артерий, выявление частоты встречаемости постэмболизационного синдрома и наиболее характерных его симптомов.
Результаты и методы исследования. Настоящее исследование проводилось на базе гинекологического отделения клиник СамГМУ. Нами были проанализированы истории болезни 84 женщин, которым проводилась эмболизация маточных артерий за период с апреля 2011 по апрель 2012гг. Средний возраст исследуемых пациенток составил 42±0,79 года. 65% (55) пациенток до операции беспокоили обильные болезненные менструации, по типу менометроррагий. 23% (19) пациенток отмечали выраженный болевой синдром внизу живота и в пояснице, 12% (10) предъявляли жалобы на нарушения функции соседних органов (учащенное мочеиспускание, или, наоборот задержку мочи). В 83% (70) случаев имело место интерстициальное или интерстициально-субсерозное расположение узлов. У 76%(53) женщин этой группы, миома матки была множественной, у 24% (17) пациенток миома матки носила единичный характер. У 17%(14) исследуемых женщин узлы располагались субмукозно.
Всем пациенткам эмболизация маточных артерий проводилась под местной анестезией. Доступ к маточным артериям осуществлялся посредством пункции правой бедренной артерии по стандартной методике Сельдингера. В качестве эмболизата использовались микроэмболы 700-1000 Нм PVA (COOK, США). Средняя продолжительность операции составила 45±0,9 мин. Для статистического анализа полученных результатов использовался метод вариационной статистики Фишер-Стьюдента. Нами оценивалось общее состояние пациенток, перенесших эмболизацию маточных артерий, наличие жалоб, а также результаты лабораторных методов исследования, в раннем послеоперационном периоде (1-10 сутки).
Средняя продолжительность госпитализации после эмболизации маточных артерий составила 6,2 койко дня. В послеоперационном периоде все пациентки получали антибактериальную терапию препаратами цефалоспоринового ряда, инфузионную терапию, анальгетики. При этом у всех исследуемых пациенток отмечался небольшой субфебрилитет, скудные мажущие выделения из половых путей. Лишь у 6%(7) пациенток отмечалась гипертермия свыше 38С°. Болевой синдром разной степени интенсивности отмечался у 100% пациенток. В основном он имел небольшую интенсивность и легко купировался анальгетиками и спазмолитиками. Однако у 4% пациенток (3) болевой синдром в первые сутки после операции был настолько выраженным, что для его купирования потребовалось назначение наркотических анальгетиков. Продолжительность болевого синдрома была не велика и составила 3-6 дней. Кроме того, в течение первых суток после операции у 12% пациенток (10) отмечались вегетативные реакции в виде тошноты, у 3 женщин, сопровождаемой рвотой 1-3 раза в сутки. Данная симптоматика легко купировалась назначением метоклопромида и инфузионной терапией.
У 1 пациентки с крупным быстрорастущим интерстициальным миоматозным узлом, диаметром 11*8,2*11 см, и исходной хронической постгеморрагической анемией средней степени тяжести, на 6 сутки после эмболизации маточных артерий развилось массивное маточное кровотечение, что привело к субтотальной гистерэктомии без придатков (общая кровопотеря составила 900 мл). Больная была выписана на 8 сутки после гистерэктомии в удоволетворительном состоянии.
При оценке результатов лабораторных анализов в общем анализе крови показатели лейкоцитоза варьировали от 11,8 до 36*10 9 л, отмечалось также повышение СОЭ в среднем до 27±8 ммч, при оценке результатов биохимического анализа крови значительных изменений выявлено не было.
Заключение. Таким образом, у 100% пациенток с миомой матки, перенесших эмболизацию маточных артерий, в раннем послеоперационном периоде встречались различные проявления постэмболизационного синдрома. Однако, в целом ранний послеоперационный период, протекал у исследуемой группы благоприятно, серьезные осложнения, потребовавшие экстренного хирургического вмешательства и гемотрансфузии отмечались лишь у 1 из 84 исследуемых пациенток.
Эмболизация маточных артерий (ЭМА) — современный метод лечения миомы матки, заключающийся в прекращении тока крови к миоме путем введения особых блокирующих веществ (эмболов).
Лечебный механизм процедуры заключается в блокировании кровотока по ветвям маточных артерий, кровоснабжающих миому. В процессе данной манипуляции сосуды, питающие здоровый миометрий, не страдают.
В основе лечебного действия ЭМА лежат анатомические особенности строения сосудов, кровоснабжающих матку и миоматозные узлы. Миома не имеет активного кровоснабжения. Артерии, идущие к миоматозному узлу, почти не соединяются с другими сосудами, и формируют так называемое перифиброидное сплетение. Кровоснабжение здоровой ткани матки происходит из нескольких артерий (в основном - маточная и яичниковая артерии), и имеет хорошо развитые коллатеральной сети.
Строение сосудов перифиброидного сплетения отличается от нормальных артерий - их диаметр в несколько раз больше, он достигает 0,5 мм. После введения препарата, содержащего эмболы в артерии перифиброидного сплетения, происходит нарушение кровоснабжения миомы, что приводит к ее фиброзу - замещению соединительной тканью. В результате этого миоматозные узлы значительно уменьшаются в размерах, или исчезают. В нормальные сосуды, питающие здоровые мышечные клетки, эмболы не попадают, т.к. такие артерии меньше эмболов по размерам. Именно на этих особенностях кровоснабжения и основан механизм ЭМА.
История метода
Впервые ЭМА начала применятся в 70-х годах 20-ого века как метод терапии маточных кровотечений, возникающих после осложненных родов либо после операций. Впервые применил эту методику для лечения миомы матки французский исследователь Жак Равина. Изначально методика предназначалась для предоперационной подготовки пациенток к удалению матки с целью уменьшения операционной кровопотери. В ходе наблюдения за женщинами после эмболизации исследователь отметил, что у большинства пациенток проявления заболевания исчезли либо значительно уменьшились, также отмечено выраженное уменьшение размеров узлов. С тех пор методика ЭМА активно изучалась, усовершенствовалась, и получила распространение по всему миру.
Техника проведения
Эмболизация маточных артерий — процедура, проводимая в тесном сотрудничестве двух специалистов – гинеколога и сосудистого хирурга. Собственно операцию выполняет хирург, так как подобное вмешательство требует большого опыта работы с ангиографическим оборудованием.
Врачом гинекологом осуществляется определение показаний к процедуре, определение сроков лечения, предоперационная подготовка, наблюдение пациентки после процедуры.
Операция проводится в операционной, оборудованной специальной ангиографической техникой. Сама по себе манипуляция практически безболезненна, поэтому общее обезболивание не применяется. В первую очередь производится пункция общей бедренной артерии, куда вводится тонкий ангиографический катетер. Далее под контролем ангиографии катетер проводится к маточной артерии с одной стороны. Через катетер вводится препарат, содержащий эмболы, которые блокируют сосуды, кровоснабжающие миому; после чего процедура повторяется с другой стороны. Эмболы представляют собой белые гранулы, состоящие из пористого пластика (поливинилалкоголя) неправильной формы и различного диаметра. Все используемые для эмболизации препараты абсолютно безопасны и не вызывают аллергической реакции. Как правило, вся манипуляция длится около 20-30 минут.
После эмболизации
Сразу после завершения процедуры у пациенток возникает ряд жалоб, которые объединены в так называемый «постэмболизационный синдром» - появляются боли в нижних отделах живота, выраженная слабость, тошнота, головокружение, повышение температуры тела. Эти симптомы являются реакцией организма на прекращение кровотока в миоме, и, как правило, не требуют лечения. Обычно этот период непродолжителен, и длится от 10 часов до нескольких дней.
В период от шести месяцев до полутора лет после ЭМА пациентки отмечают уменьшение, либо полное исчезновение всех симптомов — из-за уменьшения размеров миомы и восстановления нормальной анатомии матки отмечается нормализация менструального цикла (устраняются обильные менструации), снимается болевой синдром.
Показания для ЭМА
- миома матки, проявляющаяся крайне обильными менструациями, болевым синдромом, дизурическими явлениями, симптомами сдавления соседних органов (кроме субсерозных миом на тонком основании)
- миома матки у женщин с тяжелыми сопутствующими заболеваниями, когда имеются противопоказания к любому оперативному лечению.
- миома матки при наличии противопоказаний к гормональной терапии
- миома матки у женщин, желающих сохранить репродуктивную функцию, при невозможности эффективного выполнения консервативной миомэктомии
Противопоказания к ЭМА
- субсерозное расположение миоматозного узла.
- злокачественные заболевания эндометрия, тела и шейки матки.
- воспалительные процессы в органах малого таза, обострение хронических воспалительных заболеваний.
- беременность
- аллергия на йод (содержится в составе рентгенконтрастного вещества)
- почечная и печеночная недостаточность, препятствующая проведению рентгенконтрастных исследований.
ЭМА и беременность
Если миома матки препятствует наступлению или вынашиванию беременности, вариантами лечения выступают консервативная миомэктомия, или резектоскопия при миоме субмукозной локализации. При наличии маточного фактора бесплодия, вызванного миомой матки, данные методики неизменно показывают высокую эффективность для восстановления репродуктивной функции.
В некоторых случаях выполнение таких операций из-за расположения миоматозных узлов, их большого размера или количества невозможно или малоэффективно. Во многих случаях имеет место множественная миома матки, либо миома матки с интерстициальным (межмышечным) расположением узлов. В таких случаях попытки удалить узлы сопровождаются вмешательством в полость матки и могут привести к таким осложнениям как рубцовые деформации полости, спаечный процесс, синехии полости матки, не только не повышая шансы женщины выносить беременность, но и усугубляя их.
В таких случаях ЭМА становится методом выбора, как щадящий и органосохраняющий метод. После уменьшения размеров и фиброзирования миоматозных узлов после эмболизации происходит восстановление нормальной структуры матки, восстановление топографии цервикального канала, что улучшает репродуктивные прогнозы. В группе пациенток, у которых выполнение консервативной миомэктомии невозможно по техническим причинам, или ее проведение связано с высоким риском для здоровья, эмболизация является лучшим вариантом для сохранения и восстановления репродуктивной функции.
Осложнения
Эмболизация маточных артерий является одной из самых безопасных процедур в гинекологии, риски возникновения осложнений после нее минимальны.
К осложнениям относятся:
- формирование гематомы на бедре в месте пункции артерии. Такая ситуация не требует дополнительного лечения и проходит самостоятельно.
- аллергические реакции на рентгенконтрастное вещество (препараты, содержащие йод).
- инфекционные осложнения
- нарушение менструального цикла в течение 3-6 месяцев после процедуры, либо временная аменорея. Причиной такого осложнения является временное ухудшение кровоснабжения эндометрия после эмболизации.
Результаты процедуры и успешность ее выполнения оцениваются через 6 и 12 месяцев, за это время завершается процесс уменьшения миоматозных узлов; как правило, их объем сокращается от 40 до 70 % от исходного. При проведении ультразвукового исследования миоматозные узлы видны как плотные фиброзные образования с отсутствием кровотока, структура миометрия и кровоток в матке и яичниках при этом не страдают.
Женщинам, перенесшим эмболизацию маточных артерий, следует регулярно наблюдаться у гинеколога и проходить УЗИ органов малого таза с интервалом 6 месяцев. Вопрос о планировании беременности после эмболизации решается индивидуально в зависимости от темпов дегенерации миомы; как правило, планировать беременность можно уже через 12 месяцев после процедуры.
Актуальность проблемы
Миома матки самая распространенная опухоль у женщин, (25-30%), после 30 лет, причём ещё в репродуктивном возрасте. Основными проявлениями этого доброкачественного онкологического заболевания являются маточное кровотечение (меноррагия, метроррагия, менометроррагия), болевой синдром в области таза, обструкция мочеточника и другие симптомы [1]. Общеизвестно, что среди широкого спектра гинекологической патологии миома матки занимает ведущие позиции, частота выявления миомы матки колеблется от 10 до 35% у женщин репродуктивного возраста и возрастает до 43 — 48% у женщин в пременопаузальном возрасте [3].
Основными методами лечения миомы матки является консервативная миомэктомия, гистерэктомия и гормонотерапия. Каждый из этих методов имеет свои преимущества и недостатки. К основным отрицательным моментам можно отнести высокую частоту рецидивов и потерю репродуктивной функции после гистерэктомии [4]. Одним из методов остановки маточного кровотечения является перевязка внутренних подвздошных артерий, но операция не обеспечивает долговременный гемостаз, так как из-за быстрого развития коллатералей возникает рецидив кровотечения [6].
Наличие сочетанной соматической патологии может являться противопоказанием к медикаментозному, оперативному вмешательству, эндотрахеальному наркозу [1]. Некоторые пациентки категорически отказываются от операции из-за боязни операции, нереализованной репродуктивной функции.
В настоящее время эмболизация маточных артерий является методом выбора для остановки кровотечений из половых путей при неоперабельных образованиях матки и для предоперационной деваскуляризации сосудистых опухолей и артериовенозных аномалий с целью облегчения их хирургического удаления и снижения кровопотери [2].
Приоритет использования ЭМА при лейомиоме матки принадлежит французским исследователям. В 1995 году J.Ravina с соавт. представили работу, в которой эта методика использовалась до операции с целью уменьшения кровопотери во время последующей миомэктомии. Наблюдаемый клинический эффект позволил им применить ЭМА как альтернативу хирургическому лечению в начале у больных с крайне высоким операционным риском, а в последствии и у остальных категорий пациенток.
Эмболизация миомы матки (фибромиомы, лейомиомы, фиброида) - минимально инвазивная процедура и серьёзная альтернатива традиционной хирургической тактике. При ЭМА происходит прекращение тока крови к опухолевому узлу с развитием его инфаркта и дегенерации. В последующем, миома значительно уменьшается, её симптомы, в виде болей и кровотечений из матки, исчезают или значительно уменьшаются [9].
Большие преимущества ЭМА заключаются в следующем: ЭМА не затрагивает матку, матка, маточные трубы сохраняются нетронутыми, ЭМА сохраняет способность к деторождению, осложнения встречаются в десятки раз ниже, чем при хирургических операциях [8].
Минимальная травматичность высокоэффективных современных малоинвазивных рентгеноэндоваскулярных вмешательств позволяет уменьшить количество осложнений [7]. В Республике Татарстан ЭМА применяется с 2003 года на базе РКБ № 2 г. Казани (гл. врач Абашев А.Р.), и в настоящий момент мы располагаем опытом проведения более 511 технически успешных ЭМА. Наш опыт позволяет изучить результаты ЭМА, проанализировать технику и осложнения, встречающиеся во время проведения вмешательства и в послеоперационном периоде, а также оптимизировать методику проведения эмболизации маточных артерий у больных с миомами матки и маточными кровотечениями.
Материалы и методы
Обследовано 80 женщин с миомой матки, возраст которых колебался от 20 до 59 лет (в среднем 39,5 ± 0,5 года). Клинические проявления заболевания в виде меноррагии имели место у 71 женщин (88,7%), метроррагия – у 2 женщин (2,5%), более чем у половины пациенток (54,3%) наблюдался болевой синдром. Нарушения функции смежных органов выявлены у 14 женщин (17,5%). Длительность заболевания к моменту операции до 3х лет – 9 женщин (11,3%), от 3 до 5 лет у 51 женщин (63,7%), более 5 лет у 20 женщин (25%). Постгеморрагическая железодефицитная анемия наблюдалась у 76 женщин (92,5%). Средние размеры матки составляли (94,9 ± 5,0 мм) и не превышали 12 недель беременности. Интрамурально-субмукозная форма миомы матки диагностирована у 48 женщин (60,0 ± 5,3%). Субмукозная форма миомы матки наблюдалась у 23 женщин (28,7 ± 4,8%), множественная миома матки с интрамурально-субсерозной локализацией миоматозных узлов определена у 9 женщин (11,3 ± 3,5%).
Сопутствующие экстрагенитальные заболевания отмечены у 41 женщины (51,3 ± 5,6%). При этом гипертоническая болезнь встречалась у 5 женщин (6,3 ± 1,7%) – среди них у 2 больных в сочетании с сахарным диабетом и у 4 больных в сочетании с ожирением.
Всем больным проведено клинико-лабораторное исследование, включая коагулограмму, биохимическое исследование крови и онкомаркеров СА-125 и СА-19-9 по общепринятой методике.
Проводилось ультразвуковое исследование органов малого таза с доплерографией, позволяющее уточнить количество, структуру, локализацию миоматозных узлов. В послеоперционном периоде ультразвуковой мониторинг с целью оценки эффекта регрессии размеров миоматозных узлов.
У всех женщин были исключены острые воспалительные процессы женских половых органов.
Рентгенэндоваскулярная эмболизация маточных артерий осуществлялись в операционной, оснащенной ангиографической дигитальной цифровой установкой с плоским детектором Axiom Artis dTA (Siemens Medical System). Эмболизация маточных артерий проводиться под местной анестезией чрезкатеторной пункцией правой общей бедренной артерии в асептических условиях по методике Сельдингера и является совершенно безболезненным. По проводнику устанавливается интродюссер 5F. Для эмболизации маточных артерий стали применять модифицированную технику катетеризации маточных артерий без применения катетера Cobra для контралатерального проведения проводника в подвздошную артерию. По усовершенствованной методике катетер Roberts на гидрофильном проводнике одномоментно устанавливается в контралатеральную подвздошную артерию. После селективной установки катетера Roberts в маточную артерию, вводятся эмболизационные частицы. В качестве эмболизирующего вещества были использованы частицы эмбосферы из акрилового полимера (BioSphere Medical), имеющие размеры от 300-700 мкм. Размеры частиц позволяют полностью закрыть сосуды, окружающие и питающие миоматозные узлы. Все операции завершались контрольной артериографией таза. (Рис.1).

Рис. 1. Одномоментная катетеризация катетером Roberts контралатеральной маточной артерии
Статистическая обработка проводилась с использованием пакета программ SPSS (v.13.0). Данные представлены в виде M±m, где M - средне арифметическое значение, m – стандартная ошибка среднего значения. Отличия полагались статистически значимыми при P < 0,05.
Результаты исследования
Ангиографическое исследование выполнено всем обследованным женщинам (80 больных). При этом маточные артерии были идентифицированы как одна из ветвей передних порций внутренней подвздошной артерии в 140 из160 катетеризированных артерий. Средний диаметр маточных артерий составил 4,3 ± 0,9 мм. Образование единого ствола маточной и запирательной или маточной и пузырной артерии было выявлено в 20 клинических наблюдениях.
На всех ангиограммах были изменения, соответствующие доброкачественной гиперваскуляризации, при этом основные ветви маточных артерий образовывали округлую гиперваскулярную зону извитых сосудов без обрывов мелких артериальных ветвей, экстравазации и артериовенозного шунтировании. Накопление рентгеноконтрастного вещества в капиллярной фазе было неравномерным и усиленным, отражающим выраженный сосудистый компонент миоматозного узла и миометрия. Несмотря на это, значимого контрастирования дренирующих вен не отмечалось. Двухсторонняя катетеризация и эмболизация маточных артерий выполнялась 79 пациенткам (98,7%), тогда как у одной больной (1,3%) эмболизация маточной артерии осуществлялась на стороне преимущественного кровоснабжения (при этом диаметр контралатеральной маточной артерии был менее 1,5 мм).
Применение микрокатетера для суперселективной эмболизации маточных артерий потребовалась в 1 случае при высоком ответвлении влагалищной ветви от маточной артерии слева у одной пациентки (1,2%).
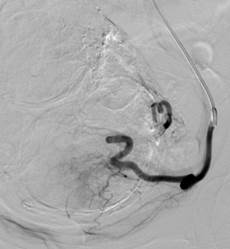
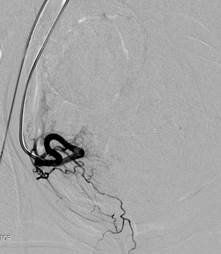
На ангиограммах артерий малого таза и маточных артерий, выполненных непосредственно во время операции до эмболизации и после эмболизации (Рис.2, А-Г), определялась полная деваскуляризация зоны патологического очага и признаки остановки (стаз контраста) кровотока по маточным артериям у 79 из 80 пациенток (98,7 ± 1,7%), тогда как у 1 пациентки (1,2 ± 0,7%) на контрольной ангиографии было выявлено частичное сохранение васкуляризации матки по маточным артериям, что потребовало повторного установления катетера и дополнительного введения эмболизирующих препаратов.
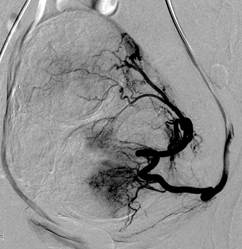
А. Ангиограмма левой маточной артерии пациентки Б., 46 лет. Множественная миома тела матки с субмукозным ростом одного из узлов с геморрагическим синдромом. Анемия 1ст. «Смешанный» тип кровоснабжения миоматозного узла.
Б. Ангиограмма левой маточной артерии после ЭМА (жидкий эмболизат) Признаки остановки (стаза) контраста, с ретроградным выбросом контраста обеих маточных артерий после процедуры ЭМА.
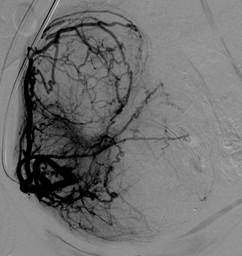
В. Ангиограмма правой маточной артерии
Г. Ангиограмма правой маточной артерии после ЭМА (жидкий эмболизат). Признаки остановки (стаза) контраста, с ретроградным выбросом контраста обеих маточных артерий после процедуры ЭМА.
Рис. 2.Этапы эмболизации маточных артерий
После эмболизации маточных артерий в раннем послеоперационном периоде у всех женщин наблюдались проявления постэмболизационного синдрома: отмечались боли внизу живота тянущего или схваткообразного характера. Наиболее выраженная интенсивность болей наблюдалась через 8 ± 0,4 часов после окончания внутрисосудистого вмешательства. Боли иррадиировали в область крестца и нижних конечностей у 12 женщин (20 ± 4,5%). Всем женщинам назначались ненаркотические анальгетики с первых суток послеоперационного периода. Наркотические анальгетики применялись по требованию только в первые 12 часов после вмешательства.
Повышение температуры тела после постоянной эмболизации маточных артерий наблюдалось у всех больных, однако более чем у половины пациенток (58,0 ± 3,9%) наблюдалась в пределах до 37,0 ºС. Продолжительность и выраженность гипертермии находились в непосредственной зависимости от размеров миоматозного узла.
Нормализация ритма и объема менструальной кровопотери и продолжительности менструации установлена у большинства больных (85,0 ± 4,6%) уже на шестом месяце наблюдения, и к концу первого года наблюдения количество женщин с восстановленным циклом и объемом менструальной кровопотери составило 76 (93,3 ± 3,2%).
Послеоперационный эффект окклюзии маточных артерий проявился трансервикальной экспульсией субмукозного миоматозного узла у 1 из 23 женщин с данной локализацией миомы матки в среднем 3,3 ± 0,4 месяца после внутрисосудистого вмешательства.
Ультразвуковое исследование органов малого таза выполнялось до и после эмболизации маточных артерий в качестве основного метода динамического наблюдения за структурой, размерами матки и миоматозных узлов.
До проведения эмболизации маточных артерий миоматозные узлы имели обычную однородную гипоэхогенную структуру с четкими ровными контурами. После эмболизации маточных артерий в раннем послеоперационном периоде (5-й день) эхографические показатели матки и миоматозных узлов достоверно не изменялись, показатели эхографической структуры миометрия были интактны. При этом средние размеры миоматозных узлов до операции составили 58,6 ± 9,6 мм., после операции 34,9±7,2 мм. через 12 месяцев. При этом средний объем миоматозных узлов соответсвенно до и после операции составили 148,1 ± 76,0 см3 и 54,2 ± 4,6 см3. Нормализация размеров матки и эхоструктуры миометрия во всех отделах матки при ультразвуковом мониторинге отмечено через 3 месяца после операции. Двусторонняя селективная эмболизация маточных артерии представляет собой эффективный метод лечения миомы матки. Преимуществами данного метода являются отсутствие общего наркоза и связанного с ним риска анестезиологических осложнений, минимальный объем кровопотери и риск осложнений, уменьшение риска рецидивов в перспективе.
Рецензенты:
Насруллаев М.Н., д.м.н., профессор кафедры хирургии ГБОУ ДПО КГМА Минздрава России, г. Казань;
Акберов Р.Ф., д.м.н., профессор кафедры лучевой диагностики ГБОУ ДПО КГМА Минздрава России, г. Казань.
В современных рекомендациях по проведению ЭМА не существует никаких ограничений по размерам миом. ЭМА возможно эффективно проводить при любом размере миомы.
Однако, в каждом конкретном случае, необходимо четко определить показания к проведению ЭМА или какого-либо другого метода лечения. Как правило, на выбор тактики влияет локализация и количество узлов, планирование беременности в будущем.
ВОЗМОЖНО ЛИ ПРИМЕНЕНИЕ ЭМА ПРИ МНОЖЕСТВЕННЫХ МИОМАХ?
Большое количество миом является одним из главных показаний к проведению ЭМА. Хирургическое удаление узлов в таких случаях, как правило невозможно. Методика проведения ЭМА позволяет лишить кровоснабжения все узлы одновременно, даже настолько мелкие, что их могли не увидеть при ультразвуковом исследовании.
В КАКОМ ВОЗРАСТЕ МОЖНО ПРОВОДИТЬ ЭМА?
Никаких возрастных ограничений не существует.
До начала менструаций миома матки не встречается. После менопаузы миома матки в большинстве случаев может регрессировать самостоятельно. Главное — это правильное определение показаний к проведению ЭМА в каждом конкретном случае.
СУЩЕСТВУЕТ ЛИ ВЕРОЯТНОСТЬ РЕЦИДИВА МИОМЫ ПОСЛЕ ЭМА?
Как и после любого другого метода лечения миом матки (кроме радикального удаления органа) после ЭМА возможно развитие рецидива.
Согласно полученным данным исследований результатов лечения большого количества пациенток с миомой матки вероятность рецидива после правильного проведения ЭМА составляет менее 10 %.
В случае возникновения рецидива возможно проведение повторной ЭМА, что позволяет уменьшить частоту возникновения рецидива практически до 0%.
КАКИЕ ИССЛЕДОВАНИЯ НЕОБХОДИМО ПРОЙТИ ПЕРЕД ПРОВЕДЕНИЕМ ЭМА?
Перед проведением ЭМА необходимо пройти ультразвуковое исследование, которое позволит определить количество, размеры узлов, их локализацию. Так же во время проведения УЗИ возможно определить характер и интенсивность кровоснабжения миоматозных узлов. Полученные данные позволят определить возможно ли проведение ЭМА или все же следует отдать предпочтение какому-либо другому методу лечения. В редких случаях может понадобиться пройти МРТ.
Для оценки состояния слизистой матки гинеколог может взять аспират из полости матки либо произвести выскабливание.
Перед проведением ЭМА необходимо сдать анализы крови и мочи (необходимый список анализов пациентка получает у доктора), пройти ЭКГ и получить консультацию терапевта.
СКОЛЬКО ДНЕЙ НЕОБХОДИМО ПРОВЕСТИ В КЛИНИКЕ?
Как правило, пациентка госпитализируется в день проведения ЭМА (предварительно пройдя необходимый перечень анализов и исследований).
После проведения ЭМА в большинстве случаев возможна выписка уже на следующий день или через день. Таким образом в клинике нужно провести 1-2 дня.
В КАКИЕ ДНИ ЦИКЛА ЛУЧШЕ ПРОВОДИТЬ ЭМА?
Согласно современных рекомендаций день цикла не играет роли в эффективности ЭМА. Однако, имеются данные, что проведение ЭМА во время месячных может сопровождаться более выраженным болевым синдромом
МОЖЕТ ЛИ ПРОВЕДЕНИЕ ЭМА ПОВЛИЯТЬ НА ЗДОРОВУЮ ТКАНЬ МАТКИ?
При правильном стандартизированном выполнении методики проведение ЭМА не оказывает никакого воздействия на здоровую ткань матки.
При этом одним из важнейших факторов является использование эмболов (мелких частичек, перекрывающих кровоснабжение миоматозных узлов) необходимого размера и формы, соблюдение характеристик «конечной точки» эмболизации.
При знании и соблюдении врачом всей технологии выполнения ЭМА повреждение эндометрия невозможно.
ЧТО ПРОИСХОДИТ С УЗЛАМИ ПОСЛЕ ПРОВЕДЕНИЯ ЭМА?
После лишения кровоснабжения узла происходит его склерозирование. При этом ткань узла, представляющая собой гладкомышечные клетки, окруженные соединительной тканью, полностью замещается соединительной тканью.
ПРИМЕНЯЮТ ЛИ ЭМА У ПАЦИЕНТОК, ПЛАНИРУЮЩИХ БЕРЕМЕННОСТЬ?
Да, применяют. Однако, согласно современных рекомендаций предпочтение к проведению ЭМА у пациенток, планирующих беременность следует отдавать только если им невозможно проведение хирургического лечения - миомэктомии (вследствие большого количества узлов, неудобной их локализации и др.).
Беременность после ЭМА возможно планировать приблизительно через 1 год, так как к этому моменту заканчивается процесс замещения узлов соединительной тканью и уменьшения их размеров.
Читайте также:

